Desvelan un mecanismo genético que permite a las neuronas cambiar su identidad según el entorno
NEUROBIOLOGÍA.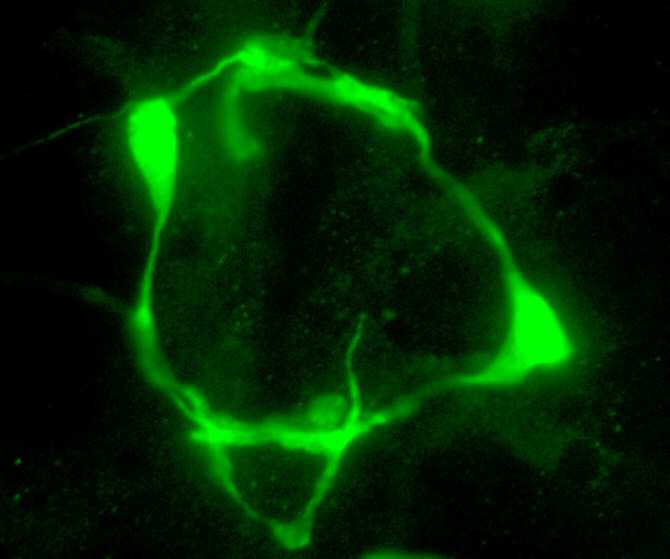
Todas las células de un organismo comparten la misma información genética (ADN), a partir de la cual surgen los diferentes tipos celulares con funciones específicas (piel, hígado, neuronas...).
Los genes y el entorno interactúan para modular las identidades y el funcionamiento de las células mediante cambios epigenéticos, un sistema que dicta a la célula cómo interpretar el ADN para funcionar de un modo concreto. Ahora, una nueva investigación ha permitido describir cómo este mecanismo regula la respuesta al neurotransmisor serotonina en un sencillo modelo animal, consiguiendo cambiar la identidad de las neuronas y su comportamiento mediante pequeños cambios en los genes en respuesta al ambiente.
Marca de serotonina en las neuronas VC de un nematodo C. elegans modificado genéticamente. Imagen: Andrea Millán-Trejo / IBV / CSIC.
El estudio es obra de un equipo encabezado por Andrea Millán-Trejo, del Instituto de Biomedicina de Valencia (IBV), adscrito al Consejo Superior de Investigaciones Científicas (CSIC) en España.
Para la investigación se usó un pequeño gusano nematodo (Caenorhabditis), un ‘laboratorio viviente’ muy empelado en biología y biomedicina para entender cómo funciona el sistema nervioso: tiene 302 neuronas, identificadas una a una. En el laboratorio que dirige Nuria Flames en el IBV, analizaron un tipo concreto de neurona de este animal (VC), que muestra indicios de algo inesperado: captar serotonina, neurotransmisor implicado en la conducta y estados internos del animal.
“En la especie Caenorhabditis elegans, las neuronas de identidad VC tienen el potencial de captar serotonina, pero no lo hacen porque existe una represión por mecanismos epigenéticos”, explica Nuria Flames. “Un mecanismo llamado metilación de histonas actúa como un candado que bloquea el gen mod-5/SERT, encargado de captar serotonina del medio. Por eso estas neuronas no muestran un fenotipo serotonérgico [firma biológica que permite a una neurona captar serotonina]”, continúa.
Identidad neuronal plástica.
El equipo de investigación comprobó que en varias especies del género Caenorhabditis, este candado se ha roto durante la evolución. “Estas especies han adquirido un nuevo ‘potenciador’ [enhancer, en inglés] que activa el gen mod-5/SERT en las neuronas VC, escapando a la represión epigenética y permitiéndoles captar serotonina de forma intensa y estable”, describe Flames. Además, basta con trasladar ese potenciador a otras especies como C. elegans para que sus neuronas VC activen el gen mod-5/SERT. “Una única pieza reguladora es suficiente para cambiar la identidad y función de las neuronas”, resume la investigadora del CSIC.
Para sorpresa del equipo, en algunas especies este cambio también se produce si lo requiere el ambiente donde habita el gusano. “Aunque, en condiciones normales, las neuronas VC de C. elegans reprimen la recaptación de serotonina, en condiciones concretas, el candado epigenético se abre y estas neuronas se vuelven serotonérgicas, lo que cambia el comportamiento de puesta de huevos. Su identidad neuronal tiene, por tanto, un carácter plástico, depende del ambiente”, revela Andrea Millán Trejo.
El uso de este modelo animal simple permite estudiar la plasticidad y la evolución de identidades celulares conectando tres niveles: regulación de genes (ADN), identidades de neuronas (células) y comportamiento (organismo). Además, muestra que no todo depende de mutaciones grandes de todo el genoma: pequeños cambios en la regulación de genes pueden tener efectos importantes.
Esto explicaría otras posibilidades de la evolución de las especies, que se produciría no solo por cambios genéticos al azar, sino también por respuestas flexibles al entorno que luego pueden volverse permanentes. Esta es la base de la asimilación genética, una teoría propuesta en la década de 1950 que hasta ahora contaba con escasa evidencia experimental sobre sus posibles mecanismos moleculares. Según esta teoría, una respuesta adaptativa y plástica provocada por el ambiente termina, tras varias generaciones, grabándose en el ADN y manifestándose de forma hereditaria sin necesidad del estímulo externo original.
Entorno y enfermedad mental.
Así, el estudio revela mecanismos de plasticidad neuronal que podrían ser comunes en animales más complejos. En este sentido, “el gen equivalente a mod-5/SERT en humanos está implicado en depresión, ansiedad o autismo”, explica Nuria Flames. “Entender cómo su expresión puede ser suprimida o activada epigenéticamente podría revelar mecanismos presentes en nuestro propio cerebro y contribuir a comprender cómo el entorno influye en la vulnerabilidad a enfermedades mentales”, avanza.
Además, explicar cómo surgen nuevas funciones en células y organismos puede ayudar a entender mejor la diversidad de los sistemas nerviosos. Puede mostrar cómo los seres vivos son capaces de adaptarse a cambios ambientales como la presencia de sustancias químicas que antes no estaban o solo existían en pequeñas cantidades, lo que podría aplicarse al estudio de la respuesta de organismos a cambios ecológicos provocados por el cambio climático global. También puede inspirar formas de controlar genes de manera flexible, activándolos o desactivándolos según el entorno, o utilizarlo como estrategia de control de gusanos parásitos en agricultura, ganadería y biomedicina.
El estudio se titula “Epigenetic constraint and enhancer innovation link neuronal plasticity to evolutionary adaptation”. Y se ha publicado en la revista académica Proceedings of the National Academy of Sciences (PNAS). (Fuente: CSIC)
Sitio Fuente: NCYT de Amazings